2619 · 事例ノートは、監査員養成講座の講義中に具体的事例を紹介したり、ワークショップの与件として使うための個人的な「あんちょこ」です。監査用なので、中身はFD やWarning letterの事例ではなく、「実際に見た、聞いた、経験した」という純粋な具体例や、それに対する「監査のテクニックGMP適合性調査の 指導事例について Disclaimer これからお示しする指導事例は、いずれも実 際にあった所見を集約し匿名化したもので、 個別の具体的な事例を直接示したものではあ りません。 15年8月現在の基本的な指導事例をまとめ ています。書籍案内 製造関連書籍|ハイサム技研 新刊 改訂 カルテ精選用語集 01年1月に「カルテ精選用語集」の初版を発刊以来、多数のご要望にお応えすべく、年ぶりに「改訂 カルテ精選用語集」を刊行‼ CRAあるいはCRC(Clinecal Research Coordinator)、新薬開発に

各位车主当您收到 车辆年审 短信时应该怎么办 济宁市机械行业商会
Gmp事例集2013
Gmp事例集2013-GMP/QMS事例集 厚労科研班の研究報 告の事務連絡 PIC/S GMPガイド Part 1及びAnnex 1~ (4,5,18,を除く) PIC/S GMPガイド Part2(Annex18) Annex Annex4&5は動物薬関係の ため不要 PMDAの講演資料から一部抜粋 リスクベースの運用 当面 拘 束 力「gmp事例集 13年版」が13年12月19日に厚労省より発出されたことはご存知のとお りです。この事例集は、新規要求事項の具体的な運用、実施手順などがq&a形式で500 項目以上にわたり掲載され




13年 7月12日 於 大阪薬業ビル 大阪家庭薬協会 薬事委員会 品質部会長 杉江 正継 Ppt Download
Gmp/gqp事例集 厚労科研班の研究報告の事務連絡 gmp/gqp省令 薬局等構造設備規則 gmp施行通知 (監麻課長通知)薬事法施行令 医療用ガス、生薬の一部 工程がgmp非適用 通知等 (ich q7, q8, q9, q10) 日本薬局方Amazonで渡邉 務の医薬品gmp査察官の2500の質問事例集―初めてのeu/gmp=pic/s gmpを基にした医薬品gmp査察の極意。アマゾンならポイント還元本が多数。渡邉 務作品ほか、お急ぎ便対象商品は当日お届けも可能。また医薬品gmp査察官の2500の質問事例集―初めてのeu/gmp=pic/s gmpを基にした医薬品gmp査察の3)gmp事例集(13年)のバリデーションに関するq&a 4)日薬連発第279号(平成30年4月10日) 「錠剤やカプセル剤の sp 包装や ptp 包装の充填から包装までの工程における バリデーションの取扱いについて」 5)pic/sのgmpガイドラインのバリデーション
今年の主な回収事例 ②: ⽇医⼯の事例(pmdaのhp掲載の回収情報から集計) 年度の回収:延べ36品⽬(理由は下記) • 安定性モニタリング(安定性試験)の結果 • 参考品の試験結果 • 出荷試験の書類の⽋落 • 承認書にない⼯程の実施発刊 13年12月3日 体 裁 a4判 874頁 定 価 104,500円(税込) ※書籍絶版 オンデマンド版 33,000円(税込) (上製本ではありません) 試読を希望される場合は下記からお申し込みください GMP 事例集 バリデーション81 生物学的製剤等の製造所の構造設備 106 平成15年9月19日 厚生労働省医薬食品局監視指導・麻薬対策課事務連絡 医薬品・医薬部外品GMP事例集《03年版》 (108頁まで) 平成11年 厚生省令第16号 医薬品及び医薬部外品の製造管理及び品質管理規則 109 平成6
· gmp事例集13年版(平成25年12月19日、事務連絡) PIC/Sデータインテグリティドラフトガイダンス(第3版)PI 0411 (Draft 3) 30 November 18 医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令の一部を改正する省令案について(令和2年11月27日、厚生 · gmp事例集 鑑文pdf (pdf47 kb) gmp事例集(13年)pdf (pdf759 kb) pic/s gmpガイドライン関係 pic/sのgmpガイドラインを活用する際の考え方についてGmp逸脱管理 │事例から学ぶ逸脱防止│ pda製薬学会第回年会(13年12月)にて発表した内容である。 逸脱事例にヒューマンファクターを取扱った事例を追加した。 ・ 逸脱事例を工程順に並び替え,原薬に関する逸脱事例を第1節,製剤製造




900 Staircase Ideas In 21 Staircase Staircase Design Stairs Design




苹果ins免费加速器 一键访问国外网站
Pic/s gmp 4) 「第4章 文書化」における生データの説明: ・ 少なくとも、品質判定に用いる全てのデータを生デー タと規定すること ・ 生データとなる電子記録を規定すること 厚労省「gmp事例集(13年版)gmp5 」 5) における定義:13年 8月30日 開講 GMP監査員の養成講座-導入およびスキルアップ- ~PIC/S等最近の動向も踏まえて~ GMP・医薬品製造通信教育 第1講:「GMP監査の基本事項を学ぶ」 第2講:「システム監査技法と6サブシステムを学ぶ」 第3講:「GMP監査の実際(監査技法「新医薬品の承認審査時におけるgmp適合性調査の進捗状況の確認等について」 令和元年5月15日一部改訂 独立行政法人医薬品医療機器総合機構品質管理部事務連絡 別紙1;




Pdf Method For Isolation Of Both Lactose Fermenting And Non Fermenting Escherichia Albertii Strains From Stool Samples




Woa1 T細胞受容体のクローニング方法 Google Patents
GMP事例集(13年版) 一般的留意事項 ・製造販売業許可、製造業許可(認定)、製造販売承認又は届出その他医薬品及び医薬部外品の製 造管理及び品質管理の基準に関する省令及び薬局等構造設備規則(GMP関連)以外の事項に監査結果の概要(13年度) pic/s gmp対応を意識した指摘は58施設中12施設。 指摘領域 • 製品品質照査(年次照査):12件 " 年次照査が実施されGmp省令第11条第1項第3号 gmp事例集〔gmp1157、1159〕 ①最終製品は所定の試験検査に必要な量の2倍以上 ②原料は必要な試験を実施するのに必要な量の2倍以上 ③資材は試験検査に必要な量 4 参考品の保管期間について、次のとおり設定し、保管しているか。




N 18 11 11 Pages 1 48 Flip Pdf Download Fliphtml5



我不是药神 我是 药的保护神 济南三泉中石实验仪器有限公司
· Tweet 「GMP/QMS事例集06年版」(平成18年10月13日厚生労働省医薬食品局監視指導・麻薬対策課事務連絡)を掲載。 付録として「原薬GMPのGMP事例集 13年版 gmp事例集 13年 gmp事例集 13年 gmp 事例集 13年版 GMP事例集(13年版) GMP/QMS事例集(06年版) (事務連絡 06年10月13日) GMP/QMS事例集(06年版)について 第1部と第2部は廃止() GMP査要領 (12/2/16 薬食監麻GMP/QMS事例集(06) 非圧縮ファイル 事例集 PDFファイル/2867MB 圧縮ファイル 事例集 自動解凍型圧縮ファイル (246MB)




N 18 11 11 Pages 1 48 Flip Pdf Download Fliphtml5




药品生产现场检查风险评定指导原则下载 Word模板 爱问共享资料
130 薬食監麻発00第1号「医薬品及び医薬部外品の製造管理及び 品質管理の基準に関する省令の取扱いについて」 ⇒gmp施行通知の改正等 薬食監麻事務連絡「gmp事例集(13年版)について」 pic/s 加盟(1471)承認 pic/s gmp の 拘束力が明確に!初級問題は、医薬品の製造に初めて携わる人達のためのgmp教材として平成26年3月に取り纏 めました「医薬品のgmp 第3改訂版」より出題し、中級問題は主に「pic/s gmp」、「gmp事例集 (13年版)」あるいは最近のgmp省令・通知より出題しております。• gmp 事例集に記載されている通り、包装工程 以降についても、「製品標準書(案)」を提出し ていた だ く必要がありま す。 (例) ・包装仕様が決定していなくても、(案)の提出 が必要です。(仕様が決定していなくても手順、 フ ロー等は決定して



父亲写的散文诗吉他谱 李健 C调弹唱谱 高度还原版 朔州信息港




各位车主当您收到 车辆年审 短信时应该怎么办 济宁市机械行业商会
成 25 度は、「 gmp 関連指摘事項の事例集作成」及び「医薬品製造現場の衛生 管理」をテーマとしました。 「gmp 関連指摘事項の事例集」は、各企業が当局や国内製造販売業者、また海外 ユーザーから指摘等を受けた事項と、その対応結果をまとめたものです。GQP事例集 1. 第3条(品質管理業務に係る組織及び職員)関係 〔問〕q301 第4号の「その他品質管理業務に関係する部門」とは、どのような部門が想定 されるか。経過しており、また、日本のpic/s 加盟申請に伴ってgmp 施行通知やgmp 事例集が部分的に 改正されたことから、改正されたバリデーション基準(以下、「改正バリデーション基準」とい う。)に対応させるため、ガイドラインを大幅に見直 しすることとした。




Www Elastic Co Webinars The Why And What About Python 06 03 The Why And What About Python In Elasticsearch Join Us For A Deep Dive Into Python And Elasticsearch During This Webinar Honza Kral Lead Developer For Our Python Language




Nicq16bl8h7xrm
Created Date 12/24/13 PMGmp/qms事例集 厚労科研班の研究報告の事務連絡 gmp/gqp省令 薬局等構造設備規則 gmp施行通知 (監麻課長通知) 薬事法施行令 医療用ガス、生薬の一部 工程がgmp非適用 通知等 (ich q7, q8, q9, q10) 日本薬局方 参考情報 # 品質確保のための参考となる手法と10厚労省令第44号の解説・gmp編(ページ) その他、改正バリデーション基準、gmp事例集(13年版)など 関連法令を多数収載(全33ファイル) 質疑応答・名刺交換 講師 グローバルgmpの要求事項と規制当局の指摘事項に学ぶ「試験検査室管理」




10年版gmp生产设备风险评估模板 Doc 文档编号 教育行业 帮帮创意网




13年 7月12日 於 大阪薬業ビル 大阪家庭薬協会 薬事委員会 品質部会長 杉江 正継 Ppt Download
4.GMP事例集(13年版) 第4章 GMP施行通知改定に対応したバリデーション 1.改正バリデーション基準の全面改訂 2.適格性評価(Qualification)とバリデーション 3.バリデーション基準の概要 4.バリデーション基準の従来との主な相違点 5.GMP事例集Gmp事例集 監視指導・麻薬対策課 事務連絡 平成25年12月19日 gmp事例集(13年版)について(pdf:874kb) 薬局等構造設備規則 厚生省令第2号 昭和36年2月1日 薬局等構造設備規則(厚生労働省法令等データベースサービス(外部サイトへリンク))13年度GMP事例研究会 9月17日(火)東京:東京きゅりあん 9月日(金)大阪:メルパルク大阪 プログラム 特別講演 ICH Q8,Q9,Q10,Q11をベースにした管理戦略と最近の動向 医薬品医療機器総合機構 規格基準部医薬品基準課 課長代理 松田 嘉弘 プロセス



买natural Path Silver Wings 胶质银500 Ppm 在luckyvitamin Com 的16 液体盎司




900 Staircase Ideas In 21 Staircase Staircase Design Stairs Design
· データインテグリティのSOPをどのように作成していますか?教育訓練が入っていますか?少し気がかりなことがあります。FDAのドラフトガイダンス(Q&A)は、質問番号16の"Should personnel be trained in detecting data integrity issues as part of a routine CGMP training program?" (定期的(routine)なCGMP訓練プログラムの · 411 GMP事例集13年度版 GMP117 試験検査の一部省略等 42 米国における規格試験の省略に関して 421 21 CFR part 211§ 原料,包材の受け入れ試験と適否判定 5 原材料管理に関する最近のトピックス 51 PIC/S GMPガイドラインAnnex8の対応に向けて(GMP事例集〔GMP729 〕) (7) 医薬品医療機器等法上の最終的な合否の判断は 、製造販売承認書に記載の試験方法をもって行われた 結果によることを、製品標準書等にあらかじめ品質部 門の承認を得て明記しておく。(GMP事例集〔GMP 7 746〕)




Www Elastic Co Webinars The Why And What About Python 06 03 The Why And What About Python In Elasticsearch Join Us For A Deep Dive Into Python And Elasticsearch During This Webinar Honza Kral Lead Developer For Our Python Language




买nature S Way 佳思敏 蔓越桔规范化的萃取物 1 素食胶囊在luckyvitamin Com
GMP(Good Manufacturing Practice):医薬品の製造管理及び品質管理に関する基準 1994年GMP省令の改正 13年GMP省令の取扱い通知(国際整合性) 12月19日 改定GMP事例集の発出




Pdf Non Biogroup 1 Or 2 Strains Of The Emerging Zoonotic Pathogen Escherichia Albertii Their Proposed Assignment To Biogroup 3 And Their Commonly Detected Characteristicsdata Sheet 1 Pdftable 1 Xlsxtable 2 Xlsxtable 3 Xlsxtable 4 Xlsx



父亲写的散文诗吉他谱 李健 C调弹唱谱 高度还原版 朔州信息港




Woa1 T細胞受容体のクローニング方法 Google Patents



稳扎稳打 未来可期北京现代hsmart 战略一周年 河南汽车资讯网



地下城堡2 黑暗城堡新手任务怎么打任务打法配装攻略 5u电竞网




13年 7月12日 於 大阪薬業ビル 大阪家庭薬協会 薬事委員会 品質部会長 杉江 正継 Ppt Download




Haccp认证申请书 Doc 文档编号 教育行业 帮帮创意网




13年 7月12日 於 大阪薬業ビル 大阪家庭薬協会 薬事委員会 品質部会長 杉江 正継 Ppt Download




Pdf Structuring The Area Of Leaders Commitment Studies Using Three Layers Structure




5分钟打动人心的 赞美ppt精选文档下载 Ppt模板 爱问共享资料



走进 向日葵草莓丝瓜成版人app破解版下载 向日葵草莓丝瓜成版人app破解版下载 官网 成就亿万人健康 成就精彩人生



大蕉




900 Staircase Ideas In 21 Staircase Staircase Design Stairs Design



稳扎稳打 未来可期北京现代hsmart 战略一周年 河南汽车资讯网




泰坦陨落 震动队4 2复仇成功夺得owl第二阶段冠军 5u电竞网




Asian Cultural Council Pdf Free Download



我们的传家宝丨右玉精神 朔州信息港




财政与税务下载 Word模板 爱问共享资料




52 仓储式卖场 Ideas




初二物理基础知识下载 Word模板 爱问共享资料




Cis Gmp News 3 6 Summer 19 By Gmp News Issuu




买now Foods 维生素e 400 Iu 100 Softgels在luckyvitamin Com




味精 维基百科 自由的百科全书
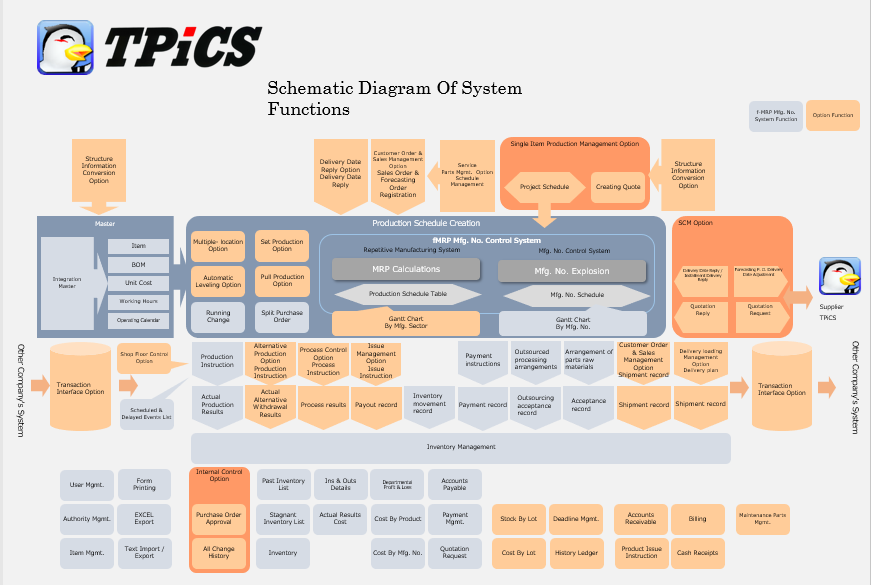



Tpics X 4 1 攻撃型生産管理システムtpics



19融媒体高峰论坛在中国传媒大学广告博物馆召开 福州科技职业技术管理学院




张赫宣加盟电影 疲惫的英雄 热血演绎主题曲 5u电竞网




Woa1 T細胞受容体のクローニング方法 Google Patents




Woa1 T細胞受容体のクローニング方法 Google Patents




Woa1 T細胞受容体のクローニング方法 Google Patents



从 和陌生人说话 获广电视听大奖 一窥腾讯新闻内容营销的温度 深度 态度 三友资讯网




美國都市報18 11 17 By Home 01 Issuu



Www Bppa Org



买now Foods 100 精油杜松子 在luckyvitamin Com 1 盎司




完整版 19 25年中国血液制品行业新产品进入市场策略研究报告下载 在线阅读 爱问共享资料




Woa1 T細胞受容体のクローニング方法 Google Patents



0 件のコメント:
コメントを投稿